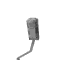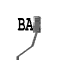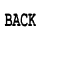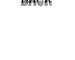
การทดลองหาปริมาณออกซิเจนในน้ำ
อุปกรณ์การทดลอง
1. น้ำจากแม่น้ำ หรือแหล่งน้ำต่างๆ (แม่น้ำน่าน)
2. กระบอกเก็บน้ำตัวอย่าง
3. บิ๊กเกอร์
4. แท่งแก้ว
5. กระบอกฉีดยา
6. สารละลาย MnSO4 2.2 mol/dm3 จำนวน 2 cm3
7. สารละลาย KI 1 mol/dm3 จำนวน 2 cm3
8. สารละลาย NaOH 12.5 mol/dm3 จำนวน 2 cm3
9. H2SO4 จำนวน 2 cm3
10. สารละลาย Na2S2O3 0.005 mol/dm3
11. น้ำแป้ง 1 cm3
1. เก็บน้ำตัวอย่างจากแหล่งต่างๆ ให้เต็มขวดขนาดประมาณ 250 cm3 โดยไม่ให้มีอากาศเหลืออยู่ในขวด ขณะเก็บอย่าให้น้ำสัมผัสกับอากาศ ปิดฝาให้แน่นแล้ว
นำไปทดลองทันที
2. นำสารละลาย MnSO4 2.2 mol/dm3 จำนวน 2 cm3 ในกระบอกฉีดยา จุ่มปลายกระบอกฉีดยาลงในน้ำตัวอย่าง โดยให้ปลายกระบอกฉีดยาอยู่ใต้ผิวน้ำ
กดกระบอกฉีดยาให้สารละลายทั้งหมดไหลลงผสมกับน้ำในขวด ปิดฝาขวดไม่ต้องเขย่า
3. นำสารละลาย KI 1 mol/dm3 ใน NaOH 12.5 mol/dm3 จำนวน 2 cm3 ในกระบอกฉีดยาแล้วเติมลงในขวดน้ำตัวอย่าง ปิดฝาขวด และกลับขวดไปมา
เพื่อให้สารละลายผสมกัน ตั้งขวดไว้เพื่อให้ตะกอนที่เกิดขึ้นตกลงมาที่ก้นขวด
4. นำ H2SO4 เข้มข้น จำนวน 2 cm3 ในกระบอกฉีดยาแล้วเติมลงในน้ำตัวอย่าง เติมกรดแล้วกลับขวดไปมา
5. นำสารละลายใสที่ได้มา 50 cm3 ใส่ในบิ๊กเกอร์ หยดสารละลาย Na2S2O3 0.005 mol/dm3 ลงไปทีละหยดจนกระทั่งได้สารละลายสีเหลืองอ่อนๆ
6. เติมน้ำแป้งประมาณ 1 cm3 เพื่อใช้เป็นอินดิเคเตอร์ แล้วไทเทรตต่อไปจนสารละลายเปลี่ยนจากสีน้ำเงินเป็นไม่มี
ผลการทดลอง
ไม่เกิดการเปลี่ยนแปลงหลังไทเทรตด้วย Na2S2O3
สรุปผลการทดลอง
จากสูตร ค่า DO = 8000/V * ความเข้มข้น Na2S2O3 (mol/dm3) * ปริมาตร Na2S2O3(cm3)
ในน้ำปกติที่มีค่า DO 3 mg/dm3 จะใช้ Na2S2O3 ความเข้มข้น 0.005 mol/dm3 จำนวน 18 cm3 ในการไทเทรต แต่จากการทดลองได้
Na2S2O3 ความเข้มข้น 0.005 mol/dm3 จำนวน 1000 cm3 ก็ยังไม่เกิดสารละลายสีเหลืองอ่อน สรุปได้ว่าน้ำจากแม่น้ำน่านมีค่า DO มากกว่า
3 mg/dm3 จัดว่าเป็นน้ำดี ไม่ใช่น้ำเสีย